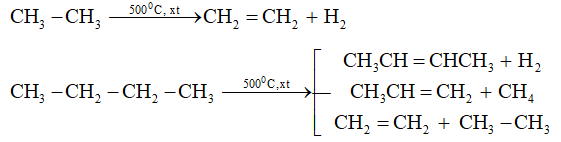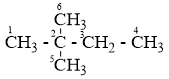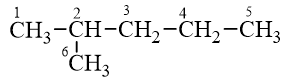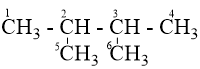C2H6 + Cl2 → HCl + C2H5Cl | Phân tích phản ứng & phương trình hóa học

C2H6 + Cl2 → HCl + C2H5Cl là một bài viết hữu ích giúp quý độc giả tiết kiệm thời gian và công sức Bài viết cung cấp thông tin về phản ứng giữa C2H6 và Cl2, điều kiện và hiện tượng phản ứng, cùng với phương trình rút gọn và bài tập vận dụng liên quan
1. Phương trình phản ứng C2H6 + Cl2:
C2H6 + Cl2 → HCl + C2H5Cl
2. Điều kiện phản ứng xảy ra:
Điều kiện phạm ứng – Xúc tác: Ánh sáng
3. Hiện tượng phản ứng giữa C2H6 + Cl2:
Cho C2H6 tác dụng với Cl2
4. Phương trình rút gọn của C2H6 + Cl2:
Phương trình rút gọn của phản ứng giữa C2H6 (etan) và Cl2 (clo) là:C2H6 + Cl2 -> 2C2H5Cl
Trong phản ứng này, etan (C2H6) phản ứng với clo (Cl2) để tạo ra hai phân tử của etyl clo (C2H5Cl).
5. Bài tập vận dụng liên quan:
Cách cân bằng phương trình:Phản ứng giữa etan (C2H6) và clor (Cl2) là một phương trình hóa học. Để cân bằng phương trình này, chúng ta cần đảm bảo rằng số lượng nguyên tử của các nguyên tố trên cả hai phía của phản ứng là tương đồng.
C2H6 + Cl2 → C2H5Cl + HCl
Phân tử etan (C2H6) bị oxi hóa bởi clor (Cl2) để tạo ra một phân tử etyl clorua (C2H5Cl) và một phân tử axit clohidric (HCl).
Để cân bằng phương trình, chúng ta phải điều chỉnh hệ số trước các chất sao cho số lượng nguyên tử carbon (C), hydro (H) và clor (Cl) cân bằng.
2C2H6 + Cl2 → 2C2H5Cl + HCl
Bằng cách nhân hệ số 2 cho C2H6 và C2H5Cl, ta có thể cân bằng phương trình trên.
Các mẹo để cân bằng phương trình hóa học chuẩn nhất:
Để cân bằng phương trình hóa học C2H6 + Cl2 → HCl + C2H5Cl, ta cần điều chỉnh hệ số của các chất sao cho số nguyên tử của các nguyên tố trên cả hai phía của phương trình bằng nhau.
Phương trình ban đầu: C2H6 + Cl2 → HCl + C2H5Cl
Nếu bắt đầu từ nội dung fragment này, kết quả sẽ là:
Ta có 2 nguyên tử carbon (C) và 6 nguyên tử hydro (H) ở phía trái, tuy nhiên chỉ có 1 nguyên tử carbon (C) và 5 nguyên tử hydro (H) ở phía phải.
Bước 1: Cân bằng nguyên tố carbon (C): Đặt hệ số 2 trước C2H6 ở phía phải để cân bằng số lượng nguyên tử carbon: C2H6 + Cl2 → HCl + 2C2H5Cl
Bước 2: Cân bằng nguyên tố hydro (H): Tạo 6 nguyên tử hydro (H) ở phía bên trái và 7 nguyên tử hydro (H) ở phía bên phải. Đặt hệ số 3 trước HCl ở phía bên phải để cân bằng số nguyên tử hydro: C2H6 + Cl2 → 3HCl + 2C2H5Cl
Bước 3: Cân bằng nguyên tố clo (Cl): Có 2 nguyên tử clo (Cl) ở phía bên trái và 1 nguyên tử clo (Cl) ở phía bên phải. Đặt hệ số 2 trước Cl2 ở phía bên trái để cân bằng số nguyên tử clo: 2C2H6 + 2Cl2 → 3HCl + 2C2H5Cl
Vậy phương trình đã được cân bằng: 2C2H6 + 2Cl2 → 3HCl + 2C2H5Cl
Cách giải phương trình:
Phản ứng hóa học mà bạn đưa ra là phản ứng giữa etan (C2H6) và clo (Cl2) để tạo ra axit clohydric (HCl) và etil clorua (C2H5Cl). Dưới đây là cách giải phản ứng này:
Bước 1: Xác định các nguyên tử trong phản ứng:
Trong phân tử etan (C2H6), chúng ta có 2 nguyên tử carbon (C) và 6 nguyên tử hydro (H).
Trong phân tử clo (Cl2), chúng ta có 2 nguyên tử clo (Cl).
Trong phân tử axít clohiđric (HCl), có một nguyên tử hydro (H) và một nguyên tử clo (Cl).
Trong phân tử etyl cloua (C2H5Cl), có hai nguyên tử cacbon (C), năm nguyên tử hydro (H) và một nguyên tử clo (Cl).
Bước 2: Cân bằng số lượng nguyên tử giữa các phía trái và phải của phương trình:
Carbon (C): 2 C (trái) = 2 C (phải)
Hydro (H): 6 H (trái) = 6 H (phải)
Clo (Cl): 2 Cl (trái) = 1 Cl (phải)
Bước 3: Cân bằng số lượng nguyên tử hydro bằng cách thêm các hệ số phù hợp vào trước các chất:
C2H6 + Cl2 → 2 HCl + C2H5Cl
Với phương trình đã cân bằng như trên, số lượng nguyên tử carbon (C), hydro (H), và clo (Cl) trên cả hai phía của phản ứng đều bằng nhau.
Mong rằng giải thích trên đã giúp bạn hiểu cách cân bằng phương trình hóa học này.
Tính chất hóa học của Ankan
Phản ứng thế
Nguyên tử H bị thế bằng halogen tạo dẫn xuất halogen:
CnH2n+2 + xCl2 → CnH2n+2-xClx + xHCl (x ≤ 2n+2)
Đối với ankan phân tử có các nguyên tử C có bậc khác nhau, sản phẩm chính thế H ở C bậc cao hơn.
CH4 + Cl2 → CH3Cl + HCl
Metyl clorua (clometan)
CH3Cl + Cl2 → CHCl3 + HCl
Metylen clorua (điclometan)
CH2Cl2 + Cl2 → CHCl3 + HCl
Clorofom (triclometan)
CHCl3 + Cl2 → CCl4 + HCl
Cacbon tetraclorua (tetraclometan)
Phản ứng tách
Tách hiđro (đề hiđro hóa): CnH2n+2 {{img_placeholder_0}}CnH2n+2-2x + xH2
Bẻ gãy các liên kết C-C ( cracking): CnH2n+2 {{img_placeholder_1}}CmH2m + Cm’H2m’+2 (n = m + m’)
Phản ứng oxi hóa (đốt cháy)
Ankan cháy tạo ra nhiều nhiệt:
CnH2n+2 + (3n+1)/2 O2 → nCO2 + (n+1)H2O
CH4 + 2O2 → CO2 + 2H2O
Câu 1. Dãy nào sau đây chỉ gồm các chất thuộc dãy đồng đẳng của metan.
A. C2H2, C3H4, C4H6, C5H8
B. CH4, C2H2, C3H4, C4H10
C. CH4, C2H6, C4H10, C5H12
D. C2H6, C3H8, C5H10, C6H12
Đáp án C
Dãy nào sau đây chỉ gồm các chất thuộc dãy đồng đẳng của metan: CH4, C2H6, C4H10, C5H12
Câu 2. Có bao nhiêu đồng phân cấu tạo mạch hở có công thức phân tử C5H12?
| A. 6 | B. 4 | C. 5 | D. 3 |
Các đồng phân ankan có CTPT C5H12 là:
CH3-CH2-CH2-CH2-CH3
CH3-CH(CH3)-CH2-CH3
C(CH3)4
Vậy có tất cả 3 đồng phân.
Câu 3. Ankan X có công thức phân tử C5H12. Clo hóa X, thu được 4 sản phẩm dẫn xuất monoClo. Tên gọi của X là
A. 2,2-đimetylprotan
B. 2- metylbutan
C. pentan
D. 2- đimetylpropan
Câu 4. Ankan X có công thức phân tử C6H14. Clo hóa X, thu được 4 sản phẩm dẫn xuất Monoclo. Tên gọi của X là
A. 2,2-đimetylbutan
B. 2- metylpentan
C. hexan
D. 2- đimetylpropan
Đáp án D
2,2-đimetylbutan
Có 3 vị trí thế Cl (C1, C3, C4) vì vị trí C1, C5, C6 là giống nhau và vị trí C2 không có H
2-metylpentan
Có 5 vị trí thế Cl (C1, C2, C3, C4, C5) vì vị trí C1 và C6 là giống nhau
n-hexan
CH3– CH2 – CH2 – CH2 – CH2 – CH3
Có 3 vị trí thế Cl (C1, C2, C3)
2,3-đimetylbutan
Có 2 vị trí thế Clo (C1 và C2) vì C2 và C3 giống nhau; C1, C4, C5, C6 giống nhau
Câu 5. Clo hóa ankan X theo tỉ lệ mol 1 : 1 tạo sản phẩm dẫn xuất monoClo có thành phần khối lượng Clo là 38,378%. Công thức phân tử của X là
A. C4H10
B. C3H8
C. C3H6
D. C2H6.
Đáp án A Câu 6. Khi đốt cháy hoàn toàn một thể tích khí thiên nhiên bao gồm metan, etan và propan với oxi không khí (trong không khí, oxi chiếm 20% thể tích), ta thu được 7,84 lít khí CO2 (đktc) và 9,9 gam nước. Ta cần ít nhất bao nhiêu thể tích không khí (đktc) để đốt cháy hoàn toàn lượng khí thiên nhiên trên?
A. 70,0 lít
B. 78,4 lít
C. 84,0 lít
D. 56,0 lít.
Đáp án A
Bảo toàn O: nO2 = nCO2 + 1/2 nH2O = 0,35 + 1/2.0,55 = 0,625 mol
Khi đốt cháy hoàn toàn một hiđrocacbon X, ta thu được 0,11 mol CO2 và 0,132 mol H2O. Khi X phản ứng với khí clo với tỷ lệ mol 1 : 1, ta thu được một sản phẩm hữu cơ duy nhất. Xin cho biết tên gọi của X.
A. 2,2-đimetylpropan
B. etan
C. 2-metylpropan
D. 2- metylbutan
Đáp án A
nCO2 > nH2O ⇒ Hiđrocacbon là ankan CnH2n+2
nankan = nH2O – nCO2 = 0,022 ⇒ n = 5. X là C5H12
X tác dụng với Cl2 tỉ lệ 1:1 thu được 1 sản phẩm duy nhất ⇒ X là: 2,2-đimetylprota
Câu 8. Đốt cháy hoàn toàn 2,9 gam ankan X, thu được 4,48 lít CO2 (đktc). Công thức phân tử của X là
A. C3H8
B. C4H10
C. C5H10
D. C5H12.
Đáp án B
Đặt công thức phân tử X là CnH2n+2
2,9n/(14n + 2) = 4,48/22,4 ⇒ n = 4
⇒ CTPT: C4H10
Câu 9. Clo hóa ankan X theo tỉ lệ mol 1: 1 tạo sản phẩm dẫn xuất monoclo có thành phần khối lượng Clo là 45,223%. Công thức phân tử của X là
A. C4H10
B. C3H8
C. C3H6
D. C2H6.
Đáp án B
CnH2n+2 + Cl2 → CnH2n+1Cl + HCl
Ta có:
35,5/(14n + 36,5) = 45,223/100 =>n = 3
X là C3H8
Câu 10. Khi cho butan tác dụng với brom thu được sản phẩm monobrom nào sau đây là sản phẩm chính?
A. CH3CH2CH2CH2Br.
B. CH3CH2CHBrCH3.
C. CH3CH2CH2CHBr2.
D. CH3CH2CBr2CH3.
Đáp án D
Butan: CH3-CH2-CH2-CH3. Khi tác dụng với brom theo tỉ lệ 1:1, brom có xu hướng thế vào H của C bậc cao
→ Công thức phân tử của X là nào?
A. CH4.
B. C2H6.
C. C3H8.
D. C4H10.
Đáp án D
Giải thích các bước giải:
Gọi công thức phân tử của ankan X là: CnH2n+2: a (mol)
Phương trình hóa học: CnH2n+2 (khí) ⟶ nC (rắn) + (n + 1)H2↑
(mol) a → (n + 1)a
Theo phương trình háo học có: nH2 = (n+ 1)nCnH2n+2 = (n + 1)a (mol)
Theo bài thu được thể tích khí gấp 5 lần thể tích ankan
=> nH2 = 5nX
→ (n+1)a = 5a
→ n+ 1 = 5
→ n = 4
Vậy công thức phân tử ankan là C4H10
Câu 12. Ứng dụng nào sau đây không phải của ankan?
A. Làm khí đốt, xăng dầu cho động cơ.
B. Làm dung môi, dầu mỡ bôi trơn, nến.
C. Làm nguyên liệu để tổng hợp các chất hữu cơ khác.
D. Tổng hợp trực tiếp polime có nhiều ứng dụng trong thực tế.
Đáp án D
Ứng dụng nào sau đây không phải của ankan:
Tổng hợp trực tiếp polime có nhiều ứng dụng trong thực tế.
Câu 13. Nhận xét nào sau đây không đúng với ankan?
A. Nhiệt độ nóng chảy tăng dần theo chiều tăng của phân tử khối.
B. Không tan trong nước, tan nhiều trong các dung môi hữu cơ.
C. Làm mất màu dung dịch thuốc tím.
D. Nhẹ hơn nước
Đáp án C Câu 14. Cặp chất nào sau đây là đồng đẳng của nhau
A. CH3OH, CH3OCH3
B. CH3OCH3, CH3CHO.
C. CH3OH, C2H5OH
D. CH3CH2OH, C3H6(OH)2.
Đáp án C