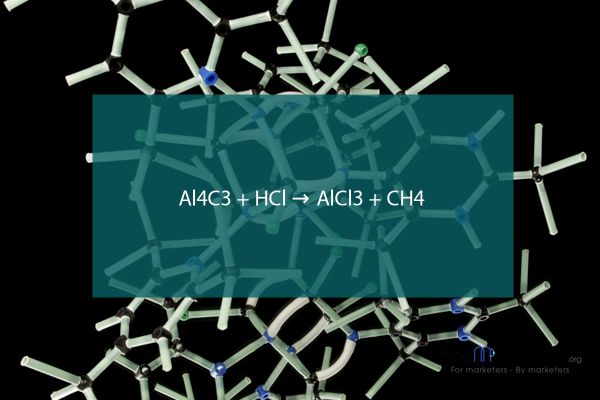
Al4C3 + HCl → AlCl3 + CH4

Nhôm cacbua (Al4C3) phản ứng với axit clohiđric (HCl) tạo ra nhôm clorua (AlCl3) và metan (CH4) Hợp chất Al4C3 được sử dụng trong sản xuất chất chống mài mòn và các sản phẩm khác
1. Phương trình phản ứng giữa Al4C3 và HCl:
Phản ứng giữa hợp chất Al4C3 và axit clohidric (HCl) là một phản ứng hóa học quan trọng được áp dụng rộng rãi trong công nghiệp và khoa học. Phương trình phản ứng có thể được viết như sau:Al4C3 + 12HCl → 4AlCl3 + 3CH4
1.1. Điều kiện phản ứng:
Trong quá trình này, sự phản ứng giữa hợp chất Al4C3 và axit clohidric sẽ tạo ra các sản phẩm gồm AlCl3 và CH4. Để phản ứng diễn ra, cần đảm bảo rằng nhiệt độ được duy trì ở mức phòng.Để thực hiện quá trình phản ứng này, chúng ta cần hòa tan hợp chất Al4C3 vào dung dịch axit clohidric. Việc này có thể được thực hiện trong một bình kín để đảm bảo tính an toàn và hiệu quả.
1.2. Cách thực hiện phản ứng:
Ngoài ra, việc sử dụng phản ứng giữa Al4C3 và HCl còn giúp sản xuất các chất hóa học quan trọng như AlCl3. AlCl3 là một chất tạo kết tủa được sử dụng để xử lý nước và trong sản xuất chất tẩy rửa. Bên cạnh đó, phản ứng này cũng có thể tạo ra khí metan (CH4), một nguyên liệu quan trọng trong sản xuất nhiều loại sản phẩm hóa học và năng lượng. Vì vậy, việc nghiên cứu và thực hiện phản ứng giữa Al4C3 và HCl có ý nghĩa quan trọng và đóng góp đáng kể cho lĩnh vực khoa học và công nghiệp.1.3. Hiện tượng nhận biết phản ứng:
Trong quá trình phản ứng, nhôm cacbua dần tan chảy trong dung dịch và giải phóng khí metan (CH4). Điều này có thể giải thích bằng việc nhôm cacbua hấp thụ ion hidroxit từ dung dịch, tạo ra các ion nhôm và cacbua. Các ion này tương tác với nhau để tạo thành chất lỏng nhôm cacbua tan trong dung dịch. Tuy nhiên, quá trình này có thể mất thời gian và năng lượng, do đó cần được kiểm soát cẩn thận để đảm bảo hiệu quả và tiết kiệm chi phí.2. Bản chất của các chất tham gia phản ứng:
2.1. Bản chất của Al4C3:
Al4C3 là một hợp chất hữu cơ gồm nhôm và cacbon, được tạo ra bằng cách nung nóng. Nó có khả năng tồn tại lâu dài và có thể phản ứng với axit clohidric (HCl), tạo ra khí metan (CH4) và clorua nhôm (AlCl3). Quá trình này có thể được mô tả như sau:Al4C3 + 12HCl → 4AlCl3 + 3CH4
Axit clohidric (
2.2. Bản chất của HCl:
HCl) là một hợp chất không cực phân tử có tính ăn mòn. Nó được sử dụng trong nhiều ứng dụng công nghiệp, bao gồm sản xuất đồ điện tử và hóa chất. Trong quá trình phản ứng, HCl tham gia vào quá trình oxi hóa Al4C3, tạo ra sản phẩm mới và tăng độ bền của hợp chất nhôm cacbua.3. Một số kiến thức mở rộng về Al4C3:
Tính chất vật lý của axit clohidric.Al4C3 là một chất rắn có màu vàng, trong suốt và có cấu trúc tinh thể hoặc phiến. Chất này có khối lượng riêng là 2,36 g/cm3 và tồn tại ở nhiệt độ lên đến 1400oC mà không bị phân hủy. Để phân biệt chất Al4C3 này, ta có thể hòa tan nó trong nước để thu được khí màu không và kết tủa keo trắng theo phản ứng hóa học sau: Al4C3 + 12H2O → 4Al(OH)3 + 3CH4.
Ngoài tính chất vật lý, Al4C3 cũng có khả năng phản ứng với nhiều chất khác nhau. Nó có thể hoà tan trong nước theo phương trình hóa học đã được đề cập ở trên. Ngoài ra, khi tác dụng với axit, Al4C3 sẽ tạo ra hai sản phẩm phản ứng là AlCl3 và CH4, có thể biểu diễn như sau: HCl + Al4C3 → AlCl3 + CH4. Nếu cho Al4C3 tác dụng với dung dịch bazơ, chúng ta sẽ thu được sản phẩm phản ứng là CH4 và NaAl(OH)2, theo phương trình hóa học sau: H2O + NaOH + Al4C3 → CH4 + NaAl(OH)2. Có những tính chất hóa học đặc biệt như vậy, Al4C3 trở thành một chất quan trọng trong nhiều lĩnh vực khác nhau.
4. Tính chất hóa học của HCl:
Ngoài tính chất vật lý, Axit clohiđric (HCl) được coi là một trong những axit mạnh nhất trong các axit vô cơ. Điều này có nghĩa là nó có khả năng tạo ra nhiều ion hiđro (H+) khi hoà tan trong nước. Dung dịch axit HCl đặc có nồng độ 37% là một dung dịch trong suốt màu trắng và có mùi hắc hơi khá khó chịu.4.1. Tác dụng chất chỉ thị:
Dung dịch HCl đặc có thể được dùng làm chỉ thị để nhận biết axit. Khi tác dụng với chỉ thị quì tím, dung dịch sẽ chuyển màu sang đỏ, cho thấy rằng nó là một axit.HCl → H+ + Cl-
4.2. Tác dụng với kim loại:
Dung dịch HCl là một chất có tính oxi hóa mạnh, có khả năng phản ứng với nhiều loại kim loại khác nhau nhằm tạo thành muối và giải phóng khí hidro. Tuy nhiên, chỉ có những kim loại đứng trước hidro trong dãy hoạt động của kim loại mới có thể phản ứng với dung dịch HCl.Ví dụ:
Fe + 2HCl → FeCl2 + H2
2Al + 6HCl → 2AlCl3 + 3H2
Cu + HCl → không có phản ứng
4.3. Tác dụng với oxit bazo và bazo:
Dung dịch HCl có khả năng tác dụng với các oxit bazơ và bazơ để tạo thành muối và nước. Quá trình này còn được gọi là phản ứng trung hòa.Ví dụ:
NaOH + HCl → NaCl + H2O CuO + 2HCl → CuCl2 + H2O Fe2O3 + 6HCl → 2FeCl3 + 3H2O
4.4. Tác dụng với muối:
Dung dịch HCl có thể tác dụng với muối để tạo ra các sản phẩm khác nhau. Quá trình này còn được gọi là phản ứng trao đổi.Ví dụ:
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
AgNO3 + HCl → AgCl↓ + HNO3 (sử dụng để phân biệt gốc clorua)
Ngoài những tác dụng trên, dung dịch axit HCl đặc còn có khả năng là chất khử khi phản ứng với các chất oxi hóa mạnh như KMnO4, MnO2, K2 Cr2O7, MnO2, KClO3...
Ví dụ:
4HCl + MnO2 → MnCl2 + Cl + 2H2O K2Cr2O7 + 14HCl → 3Cl2 + 2KCl + 2CrCl3 + 7H2O
Hỗn hợp gồm 3 phần HCl và 1 phần HNO3 đặc được gọi là nước cường toan, có thể hoà tan vàng (Au). Nó còn được gọi là "nước cường". Ví dụ:
3HCl + HNO3 → 2Cl + NOCl + 2H2O
NOCl → NO + Cl
Au + 3Cl → AuCl3
Ngoài ra, dung dịch axit HCl đặc còn được sử dụng trong nhiều lĩnh vực khác nhau, bao gồm sản xuất chất tẩy, phân tích hóa học và làm sạch kim loại. Tuy nhiên, vì tính chất ăn mòn mạnh, việc sử dụng dung dịch axit HCl yêu cầu phải tuân thủ các biện pháp bảo vệ an toàn và môi trường.
4.5. Bạn có biết:
Canxi cacbua cũng có phản ứng với axit clohidric
5. Bài tập ôn luyện:
Câu 1. Điều khẳng định nào sau đây không đúng:A. Metan là chất khí nhẹ hơn không khí.
B. Metan là nguồn cung cáp hiđro cho công nghiệp sản xuất phân bón hoá học.
C. Metan là chất khí cháy được trong không khí, toả nhiều nhiệt.
D. Metan là chất khí nhẹ hơn khí hiđro
Đáp án D
Câu 2: Hiện tượng nào xảy ra khi cho từ từ đến dư dung dịch NaOH vào dung dịch AlCl3 ?
A. Ban đầu không thấy hiện tượng, sau đó kết tủa xuất hiện.
B. Xuất hiện kết tủa keo trắng ngay lập tức, sau đó kết tủa tan dần.
C. Ban đầu không thấy hiện tượng, sau đó kết tủa xuất hiện, rồi tan dần.
D. Xuất hiện kết tủa keo trắng ngay lập tức và không tan.
Đáp án: B
Câu 3: Trong các cặp chất sau đây, cặp chất nào có thể cùng tồn tại trong một dung dịch?
A. AlCl3 và Na2CO3
B. HNO3 và NaHCO3
C. NaAlO2 và KOH
D. NaCl và AgNO3
Đáp án: C
Hướng dẫn giải
NaAlO2 và KOH không xảy ra phản ứng hóa học
Câu 4: Dùng hóa chất nào sau đây để phân biệt Zn(NO3)2 và Al(NO3)3 ?
A. Dung dịch NaOH
B. Dung dịch Ba(OH)2
C. Dung dịch NH3
D. Dung dịch nước vôi trong
Đáp án: C
Hướng dẫn giải
Câu 5. Để kiểm chứng xem phản ứng cháy giữa metan và oxi có tạo thành khí cacbonic hay không, ta cần sử dụng chất hóa học nào trong ống nghiệm?
A. H2O
B. dung dịch Ca(OH)2
C. dung dịch NaOH
D. Thuốc tím
Đáp án B
Câu 6. Để có thể thu được khí CH4 trong phòng thí nghiệm, người ta sử dùng cách nào sau đây
A. Đẩy không khí (ngửa bình)
B. Đẩy axit
C. Đẩy nước (úp bình)
D. Đẩy bazo
Đáp án C
Câu 7. Khi cho nhôm cacbua (Al4C3) tác dụng với HCl thì thu được sản phẩm gồm:
A. C2H6 và AlCl3
B. CH4 và AlCl3
C. C2H4 và AlCl3
D. C3H8 và AlCl3
Đáp án B
Câu 8. Đốt cháy hết 2,24 lít khí metan trong không khí thu được V lít khí CO2. Giá trị của V
A. 2,24 lít
B. 4,48 lít
C. 3,36 lít
D. 6,72 lít
Đáp án A
Câu 9. Nhận xét nào sau đây không đúng
A. Metan là khí không màu ,không mùi,tan tốt trong nước
B. Metan có phản ứng thế với clo
C. Trong phân tử Metan có 4 liên kết đơn
D. Metan cháy trong oxi và tỏa nhiều nhiệt
Đáp án A






